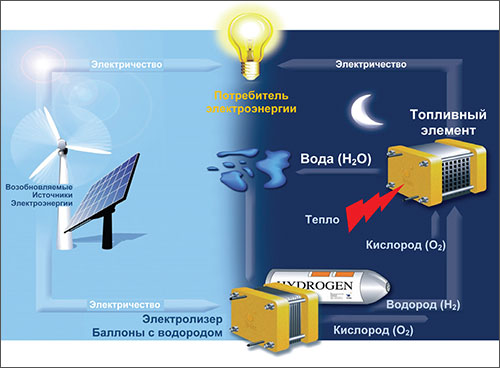
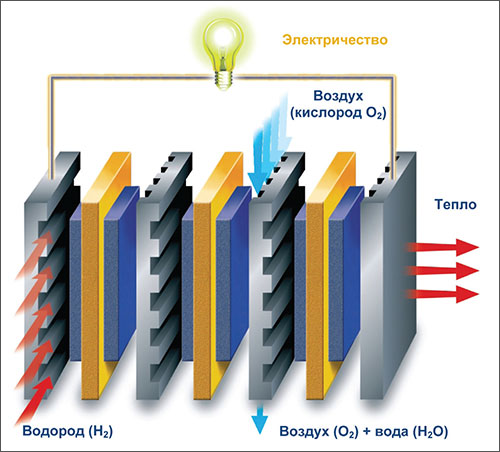
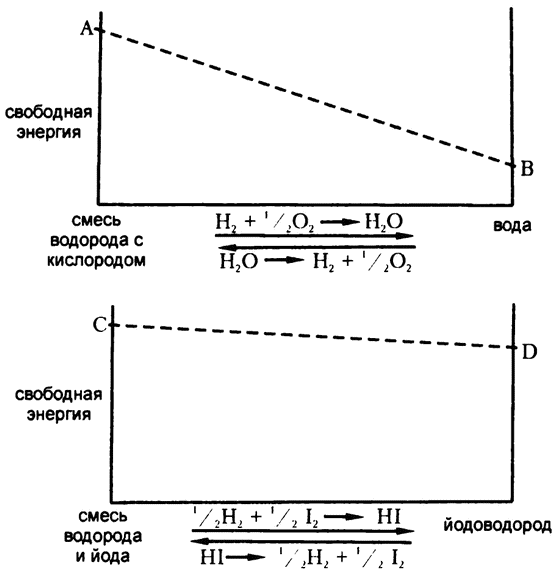
Электричество из водорода и кислорода

Количество электричества для выделения 2 г водорода из раствора
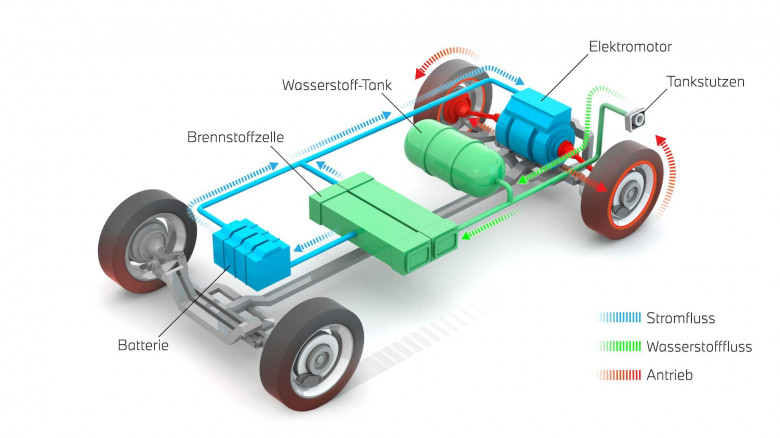
Водородная энергетика — отрасль энергетики , основанная на использовании водорода в качестве средства для зарядки, транспортировки, производства и потребления энергии. Водород выбран как наиболее распространенный элемент в космосе, теплота сгорания водорода максимальная, а продуктом сгорания в кислороде является вода которая также вводится в оборот водородной энергетики. Водородная энергетика относится к альтернативной энергетике , если водород производится с помощью возобновляемых источников энергии. На настоящий момент наиболее экономически выгодным считается производство водорода из ископаемого сырья. Снизить уровень выбросов углерода в производственных отраслях можно за счет водорода, полученного с использованием низкоуглеродных технологий, для этого можно применять технологии улавливания и хранения углекислого газа, а также электролиза воды, «в первую очередь с помощью энергии объектов атомной, гидро-, ветряной и солнечной энергетики».







PRO бизнес:. Водород считается самым простым химическим веществом, однако все не так просто. Попытки использования водорода в качестве средства для получения энергии привели к появлению нового направления — водородной энергетики. Возобновляемые источники энергии ВИЭ. Распечатать Отправить по E-mail. Открытое интервью: Сергей Переслегин, российский футуролог.




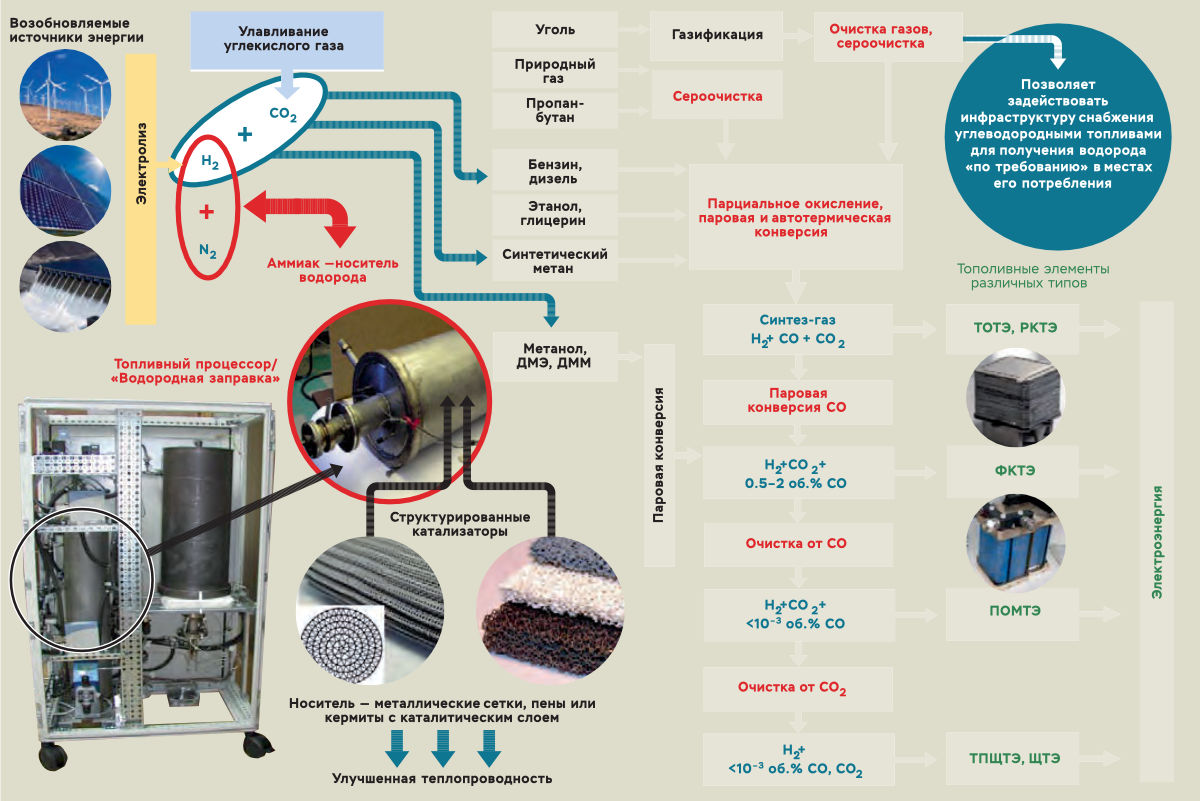


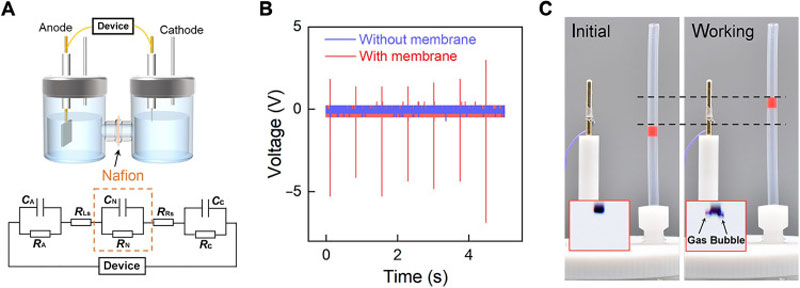
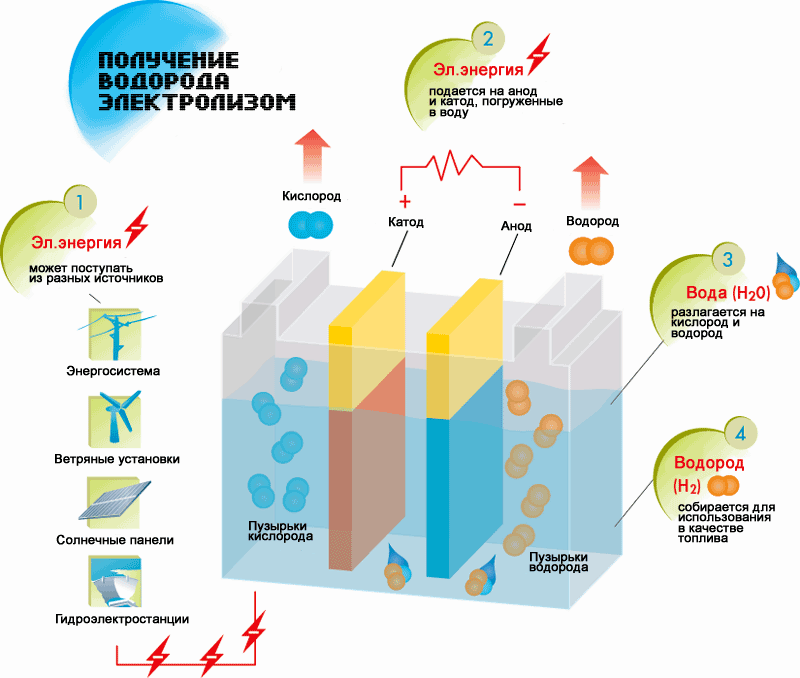
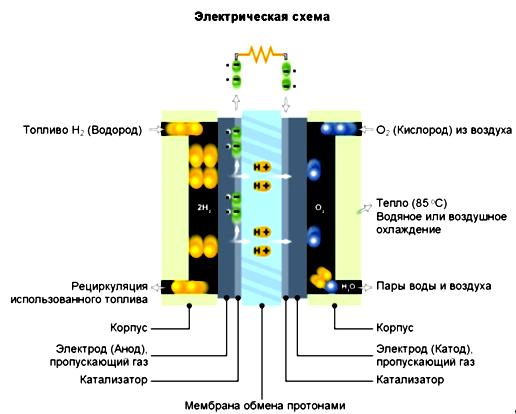


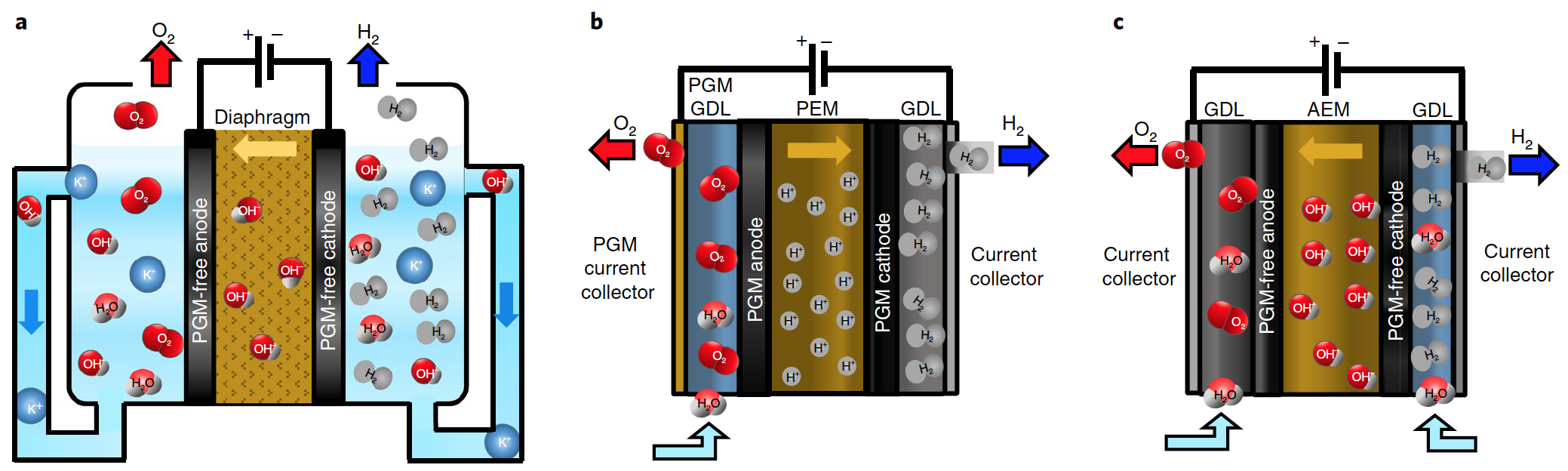
Электролиз воды — использование электричества для расщепления воды на кислород O 2 и водород H 2 путем электролиза. Выделяющийся таким образом газообразный водород можно использовать в качестве водородного топлива , но его следует хранить отдельно от кислорода, поскольку их смесь гремучий газ будет чрезвычайно взрывоопасной. Источник питания постоянного тока подключается к двум электродам обычно сделанным из инертного металла , таких как платина или иридий , помещенных в воду. В процессе электрохимического разложения воды на катоде где электроны попадают в воду появляется водород, а на аноде — кислород [1].








